Изменить чье-то генетическое программирование легче, чем вы думаете. В то время как методы изменения ДНК на молекулярном уровне становятся все более широко используемыми, также возможно просто включать или выключать гены без постоянного изменения основного генетического материала. Это означает, что мы можем влиять на генетические инструкции, которые отправляются в организм организма, изменяя его окружающую среду или с помощью лекарств.
Эта область «эпигенетики» уже помогает врачам понять, как работают определенные заболевания, почему физические упражнения могут быть такими полезными, и как мы можем изменить процесс старения. Но мы с коллегами пытаемся выяснить роль эпигенетики у бактерий.
Недавно мы изучили возможный способ воздействия на бактериальную эпигенетику, который мог бы остановить инфекцию без использования антибиотиков. А учитывая, что многие бактерии становятся устойчивыми к существующим антибиотикам, это может открыть новый жизненно важный способ лечения заболеваний.
В нашем исследовании изучалась бактерия Acinetobacter baumannii, которая является основной причиной инфекций, которые люди могут заразить в больницах, и которая убивает до 70 процентов людей, инфицированных ею. Антибиотики больше не действуют на некоторые штаммы A. baumannii - и Всемирная организация здравоохранения недавно определила его как наибольшую бактериальную угрозу для здоровья человека.
У нас уже есть некоторые так называемые противовирусные препараты, которые не убивают бактерии, но делают их безвредными, так что иммунная система организма может их очистить, не оставляя позади, чтобы стать резистентными к препарату. Если мы найдем способ повлиять на эпигенетику бактерий и обезопасить насекомых, это поможет нам создать новые противовирусные препараты, которые внесут огромный вклад в медицину.
Чтобы начать этот процесс, мы сначала обратились к эпигенетике человека. Самый распространенный способ повлиять на нашу эпигенетику - это добавить небольшую молекулярную метку к нашему генетическому материалу, которая включает или выключает связанный ген. В частности, мы можем добавить метку, известную как ацетильная группа, к важному белку, называемому гистоном.
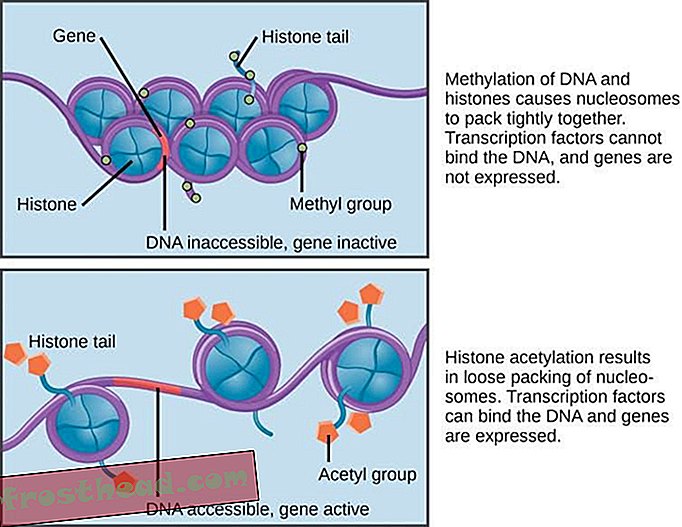 Добавление ацетильной метки к гистону (CNX OpenStax, CC BY)
Добавление ацетильной метки к гистону (CNX OpenStax, CC BY) Гистон организует наши молекулы ДНК длиной 2 метра, чтобы они могли аккуратно вписаться в наши клетки длиной 100 микрометров. Добавление ацетильной метки является естественным механизмом, используемым клетками для изменения способа взаимодействия гистона с ДНК. Добавление ацетильных меток обычно активирует определенные гены, то есть они изменяют поведение клетки. Неудачи в этом процессе модификации гистонов связаны с раковыми заболеваниями, сердечно-сосудистыми заболеваниями и многими нейродегенеративными нарушениями.
Бактериальные клетки имеют свою собственную версию гистона, известного как HU, который организует свою ДНК и участвует в работе всех своих функций. Бактерии, которые называются «грамположительными», например бактерии в нашей пищеварительной системе, которые помогают нам расщеплять пищу, не могут выжить без работы HU. А «грамотрицательные бактерии», которые, как правило, вызывают у нас болезни, такие как Salmonella enterica, становятся гораздо менее вредными без HU.
Новые лекарства
В нашем исследовании мы обнаружили, что добавление ацетильной метки к HU значительно влияет на то, как она взаимодействует с ДНК. Это означает, что весьма вероятно, что такая модификация вносит эпигенетические изменения, влияя на то, как бактерии растут и заражают другие организмы. Поэтому, если мы сможем создавать лекарства, которые вносят эти изменения в бактериальные белки таким образом, у нас мог бы быть новый способ остановить инфекции.
Это действительно важная задача в медицине сейчас, потому что бактерии, устойчивые к антибиотикам, убивают 700 000 человек в год во всем мире. Если мы не найдем новых методов лечения, к 2025 году ежегодное число погибших может возрасти до 10 миллионов.
Как только мы проверим связь между определенными эпигенетическими изменениями и бактериальной инфекцией, мы можем начать поиск веществ, которые таким образом изменяют эпигенетику бактерий, чтобы сделать их менее вредными. Уже есть несколько молекул, нацеленных на эпигенетику человека подобным образом в ходе доклинической разработки или в клинических испытаниях. Таким образом, лекарство, которое «отключает» способность бактерий вызывать инфекции, может быть не слишком далеко.
Эта статья была первоначально опубликована на разговор.
Ю-Сюань Цай, преподаватель органической химии, Университет Кардиффа