В молодом возрасте у Этана был диагностирован умеренный или тяжелый аутизм. К семи годам, несмотря на героические усилия семьи и специалистов по реабилитации, его словарный запас, диета и социальные взаимодействия были чрезвычайно ограничены. Он даже не был приучен к горшку.
Однажды утром, всего через четыре недели после специального клинического испытания, мать Этана, Дана, проснулась с широкой улыбкой на лице, говоря: «Доброе утро, мама». Превращение было чудесным, сторона ее сына, которую она никогда раньше не видела, и она заплакала от радости.
Это было чудо какашки. Не совсем сырые вещи из туалета, а скорее переработанные кишечные микробные организмы от тщательно проверенного донора, который Этан принимал в своих напитках в ходе испытания.
«Существует очень высокая корреляция между тяжестью [желудочно-кишечного тракта] и тяжестью аутизма - для языка, для социального взаимодействия, для поведения - всех основных симптомов аутизма», - говорит Джим Адамс, профессор и исследователь аутизма в Университете штата Аризона. Он Я видел связь из первых рук, когда его дочери поставили диагноз РАС: «Вопрос в том, из-за боли и дискомфорта в желудочно-кишечном тракте, или это нечто большее?»
Когда Адамс углубился в научную литературу, он обнаружил, что дисбиоз или нарушение нормальной экосистемы бактерий и других организмов в кишечнике могут влиять как на симптомы РАС, так и на ЖКТ. Лечение ванкомицином, мощным антибиотиком, который не всасывается в кровь, а остается в кишечнике, может принести временное облегчение. Но антибиотик может быть использован только в течение короткого периода времени, прежде чем бактерии начинают развивать устойчивость к нему.
Более десяти лет назад появилась теория о связи кишечника с мозгом, в которой дисфункция кишечника также может влиять на активность мозга. «Семьдесят процентов наших нервов, которые входят в центральную нервную систему, попадают в нашу кишку. Почему это так? »- спрашивает Саркис Мазманян, медицинский исследователь из Калифорнийского технологического института. Мазманян отметил, что у мышей без микробов, в кишечнике которых нет бактерий, «такие вещи, как беспокойство, локомоция, депрессия и даже развитие мозга, по-видимому, изменены» по сравнению с нормальными животными.
Мазманян и группа исследователей продемонстрировали эту связь кишечника с мозгом на мышиной модели аутизма в 2013 году. Три года спустя команда сделала то же самое для болезни Паркинсона. И недавно они показали, что пересадка фекалий от человека с аутизмом мышам без микробов вызывает у животных много симптомов аутизма.
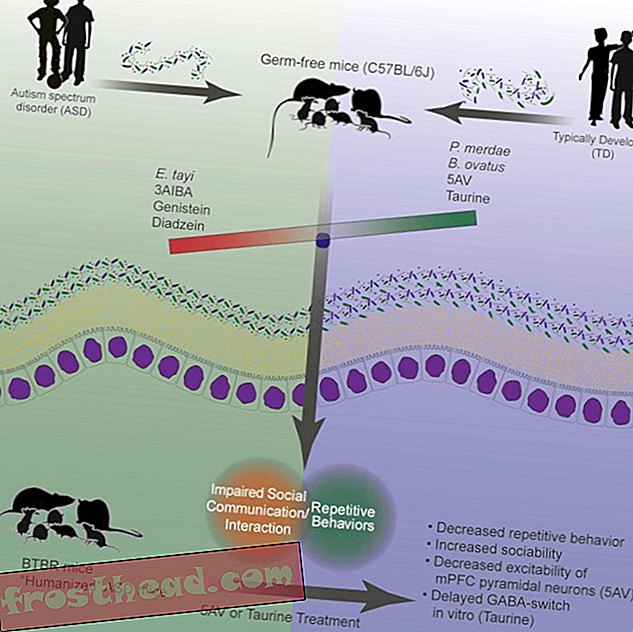 После пересадки образцов микробиома от людей с РАС мышам без микробов у мышей наблюдались поведенческие симптомы аутизма. После дальнейшей обработки микробиомом мыши демонстрировали повышенную общительность. (Гил Шарон и др. / Cell 2019.05.004)
После пересадки образцов микробиома от людей с РАС мышам без микробов у мышей наблюдались поведенческие симптомы аутизма. После дальнейшей обработки микробиомом мыши демонстрировали повышенную общительность. (Гил Шарон и др. / Cell 2019.05.004) Здоровая кишечная экосистема содержит около тысячи различных видов бактерий, а также архей, грибов и вирусов, хотя конкретные организмы и их количество могут варьироваться от человека к человеку. Напротив, разнообразие бактерий, обнаруживаемых у людей с РАС, примерно на 25 процентов ниже, чем у здоровых людей. В их кишках отсутствуют сотни различных видов бактерий, часто тех, которые важны для ферментации и выработки короткоцепочечных жирных кислот, влияющих на здоровье.
Адамс надеялся собрать воедино все нити этих различных направлений исследований, проведя исследование эффективности фекальных трансплантатов у детей с РАС. Его команда в ASU, Исследовательская программа Аутизма / Аспергера, наняла эксперта по выявлению бактерий в кишечнике, Розу Краймалник-Браун, более известного как доктор Рози. Мало что было известно о пересадке кала у детей в то время, когда было предложено исследование, поэтому FDA сначала требовало небольшое предварительное исследование безопасности, ограниченное детьми в возрасте семи лет и старше.
В исследование были включены 18 детей в возрасте от 7 до 18 лет с диагнозом РАС и значительными проблемами желудочно-кишечного тракта. Режим был требовательным, но относительно дружелюбным к детям. Сначала был использован антибиотик ванкомицин, чтобы снизить количество микробов в их кишках. Затем дети получали ежедневные дозы очищенных микробов от кишок здоровых доноров, которые были суспендированы в жидкости и смешаны с напитками вместе с антацидом для уменьшения кислот желудка, которые могут разрушить микробы, прежде чем они достигнут кишечника. Лечение кишечника продолжалось в течение десяти недель.
Поначалу исследователи ASU не увидели большого отклика. Вполне вероятно, что первоначальный дисбактериоз повредил некоторые из клеток, выстилающих кишку, как это происходит у пациентов с синдромом раздраженного кишечника (СРК), и потребовалось некоторое время, чтобы эти раны восстановились достаточно, чтобы поддержать колонизацию донорскими бактериями. Но на полпути режима большинство участников показали все больше признаков улучшения.
Только два участника показали минимальный ответ, примерно 30-процентное улучшение их симптомов ЖКТ, и это длилось недолго после завершения лечения. Но у 16 детей по меньшей мере 70-процентное улучшение их симптомов GI, и, что важно, они показали улучшение своих поведенческих симптомов аутизма. Эта статья была опубликована в январе 2017 года и настолько впечатлила Пентагон, что министерство обороны согласилось профинансировать большое исследование по микробной трансплантации у взрослых с аутизмом, в которое начали поступать пациенты в начале 2018 года.
Адамс был удивлен, услышав, что родители говорят, что их дети продолжали демонстрировать улучшение поведения, связанного с РАС, даже после завершения исследования. Команда решила провести двухлетнее наблюдение, чтобы увидеть, что происходит.
Независимый профессиональный оценщик, использующий Шкалу оценки детского аутизма (CARS), обнаружил, что симптомы были на 23% менее серьезными в конце лечения, чем в начале; два года спустя это улучшилось до 47 процентов. Первоначально 83 процента участников были оценены по тяжелой шкале шкалы ASD, но после двухлетнего наблюдения это число упало до 17 процентов, в то время как 44 процента улучшились до такой степени, что они упали ниже диагностического предела ASD.,
Измерения с использованием оценки по шкале социальной ответственности (SRS), оцененной родителями, показали параллельные улучшения, согласно последующему документу, опубликованному в апреле этого года. Похоже, что кишечный микробиом может предоставить новый инструмент для лечения РАС.
После наблюдения участники по-прежнему демонстрировали здоровое разнообразие микробиомов, но популяции бактерий в их кишках отошли от напоминания о доноре и стали более персонализированными. Изменения отражают диеты, воздействие окружающей среды, иммунную систему и генетику, уникальные для каждого человека.
«Аналогия в том, что когда у вас есть компания с отличной рабочей средой, хорошие люди хотят прийти и работать в этой компании», - говорит Краймалник-Браун. «В кишечнике, если у вас хорошая среда, у вас есть хорошие микробы, и другие хорошие микробы тоже хотят прийти и быть там».
Однако команда не утверждает, что все улучшения происходят от лечения кишечных бактерий. В то время как Адамс полагает, что восстановление здорового кишечного микробиома приносит пользу оси кишечника-мозга, которая стала изогнутой при РАС, он также считает, что простое устранение боли и отвлечения дисбиотической кишки может помочь детям сосредоточиться, сосредоточиться и извлечь выгоду из речи, поведения и другие методы лечения, предлагаемые государственными и социальными организациями.
«К сожалению, эти симптомы GI обычно игнорируются, даже когда родители детей с аутизмом сообщают, что поведение их ребенка улучшается, когда они лечат эти симптомы», - говорит Пол Эшвуд, микробиолог, изучающий ASD в Университете Калифорнии в Дэвисе. Он признает ограничения исследования Адамса и Краймалника-Брауна, такие как малый размер выборки и влияние внешних факторов, но говорит, что «данные очень интересны и должны быть изучены».
Как и в случае любого нового подхода к лечению медицинского состояния, первоначальный успех вызывает больше вопросов, чем ответов. Будет ли этот метод полезен для более широкой группы пациентов с РАС, включая тех, кто не страдает значительным дистрессом желудочно-кишечного тракта? Нужен ли ванкомицин для разрушения существующей микробной экосистемы до притока здоровых кишечных бактерий? Какова лучшая продолжительность лечения? Чтобы ответить на эти вопросы, потребуется время и многократные исследования, но Адамс с оптимизмом смотрит на то, что через несколько лет будет доступно лицензированное микробное лечение аутизма.
Тем временем команда ASU готовит еще одно испытание для детей. Их сотрудники разработали таблеточную форму микробного трансплантата, которая, по их мнению, обойдет проблему с желудочной кислотой и доставит более устойчивый продукт в кишечник. Таблетка уже используется в других исследованиях, и Адамс полагает, что изменение даст более последовательные результаты, чем их первое испытание.
Со своей стороны, Дана в восторге от «фантастического прогресса», который Этан, которому сейчас 12 лет, продолжает добиваться. Он достиг всех целей, поставленных речевыми и профессиональными терапевтами, и продолжает работать над социальными и жизненными навыками, такими как изучение того, как понимать свои собственные эмоции и чувства других и формулирование того, что он чувствует. Если медицинские исследователи, такие как команда ASU, смогут продолжать делать успехи в разработке лечения микробиома при РАС, многие дети могут извлечь пользу из разнообразной ценности здорового кишечника.